Chaulage
Chaulage et amendements basiques
Mode d’emploi : la nouvelle approche de la maîtrise de l’acidité des sols, issue des travaux du groupe chaulage du COMIFER, recentre les problèmes du chaulage.
Sommaire
Les amendements basiques - propriétés
Ils sont constitués :
- d’un anion portant des charges négatives capable de s’associer avec les H+ pour les neutraliser (propriétés basiques). Parmi ces anions on peut citer O2- constitutif de la chaux vive CaO, HO- anion de la chaux éteinte Ca(OH)2, CO32- anion du carbonate de calcium (CaCO3) ou de magnésium (MgCO3).
- d’un cation portant des charges positives et pouvant s’adsorber sur les sites négatifs du complexe adsorbant. Parmi ces cations, Ca2+ (calcium), Mg2+ (magnésium) sont les plus courants.
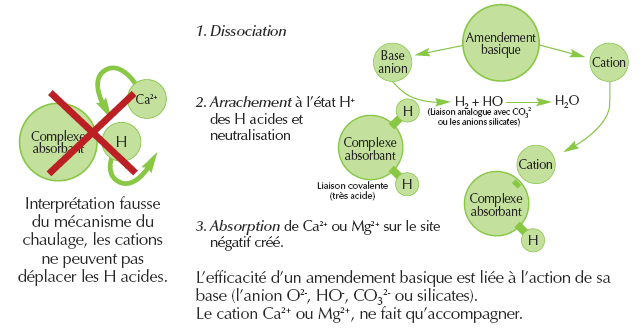
Les amendements basiques - mode d’action
Seules les bases issues de l’amendement basique peuvent “arracher” et neutraliser les H acides fixés sur le complexe. Le pH du sol augmente. Les sites négatifs, libérés par les H+, peuvent alors accueillir les cations Ca2+ ou Mg2+ apportés par l’amendement.
Conséquences :
- Le pH augmente du fait de la neutralisation de H+.
- La présence d’ions aluminium échangeables et en solution (si pH inférieur à 5,8) diminue, du fait de la précipitation de l’aluminium avec libération de sites négatifs.
- La CEC effective augmente (sites négatifs plus nombreux).
- La quantité de calcium échangeable (voire de magnésium) augmente.
Calcul des besoins en amendements basiques
Cas général : les besoins de bases (chaulage) se raisonnent à partir de plusieurs indicateurs du statut acido-basique du sol.
Description des principaux indicateurs retenus
| Indicateur |
Description |
Avantages |
Limites |
Explications agronomiques |
pH eau |
Mesure l’acidité d’une suspension de terre dans l’eau (rapport terre/eau normalisé) |
Mesure simple peu onéreuse Nombreuses références agronomiques |
Fortes variations dans l’année (plus élevé en hiver que l’été)(1) et variations spatiales |
Plus le pH est bas, plus la concentration en ions H+ et en aluminium dans la solution du sol est élevée (risque de toxicité) |
CEC Metson |
Capacité d’Echange en Cations, extraction à pH 7 par l’acétate d’ammonium |
Méthode universelle de référence |
Sur sols sableux forte variation |
Mesure la charge négative potentielle du sol (pH = 7) |
S/T ou taux de saturation |
|
Corrélé avec le pH eau, un des estimateurs du besoin en « chaux » |
Entretien l’idée fausse de l’effet basique de ces 4 cations |
Mesure la part potentielle (pH = 7) occupée par les cations |
Ca/T ou taux de saturation en calcium |
|
Idem, mais limité au calcium |
Idem, ci-dessus |
Mesure la part occupée par le calcium |
Aluminium échangeable |
Mesure conventionnelle de l’aluminium échangeable du complexe absorbant |
Un des indicateurs de la toxicité aluminique |
Ne permet pas de quantifier le besoin en « chaux » |
En équilibre avec les ions aluminium en solution, dont certains sont toxiques pour les plantes |
(1) Variations dépendant de l’activité biologique, des précipitations, de la fertilisation…
(2) Cations et CEC exprimés en meq/100g ou Cmol+/kg
Interprétation des indicateurs à partir de valeurs moyennes
| Domaine |
Très acide |
Acide |
Peu acide |
Neutre |
| pH eau | 5,5 |
5,8 |
6,5 |
7,2 |
| S/CEC (%) | 55 |
70 |
100 |
> 100 |
| Ca/CEC (%) | 45 |
55 |
85 |
> 100 |
| Complexe absorbant | Ions aluminium dominants |
Ca, Mg et K dominants Al surtout complexé |
Saturé par Ca, K et Mg Aluminium complexé et précipité | |
| Solution du sol | Aluminium abondant (toxicité +) |
Peu d’aluminium (toxicité -) |
Absence d’aluminium, Ca variable, pas de toxicité | |
Estimation des besoins de bases
Cas général
- Eléments pris en compte pour le calcul du redressement :
- pH eau = 5.8
- CEC Metson = 12 cmol+/kg
- S /CEC = 68 %
- Profondeur du sol = 30 cm, absence de cailloux, soit un poids de terre fine estimé à 3700 tonnes/ha
- Objectifs de l’apport d’amendement :
- Atteindre un pH de 6.3 optimum pour une céréale,
- Soit le S/CEC souhaitable de 90 % (pH eau et S/CEC sont très bien corrélés)
- Besoin de bases (BDB) :
BDB = CEC x (S/CEC opti - S/CEC analyse) x 0.28 x Pds de terre fine
Pour cet exemple : BDB arrondi = 2750 unités de valeur neutralisante/ha
Cet apport pourra être fractionné en 2 fois, en apportant un amendement basique calcique (et magnésien en cas de déficit en magnésie).
Cas particulier des sols sableux
- Estimation du redressement :
Si la CEC est inférieure à 5, on considère que les rapports des éléments sur la CEC deviennent peu significatifs. En conséquence, le calcul du Besoin de Bases (BDB) ne s’effectue plus à partir du [S/CEC] mais à partir du pH, suivant la formule suivante :
BDB = a x Mat.Org + b x (6.0 - pHanalyse) - c
(Pour un pH optimum de 6 : a=28.7 ; b =1410 ; c =830)
- Stratégie de fertilisation :
- Les risques de toxicité aluminique sont élevés jusqu’au pH de 5.
- Si le pH < 6.0, on prévoit un redressement (BDB) plus entretien.
- Si le pH est entre 6 et 6.2, on ne prévoit qu’un entretien tous les 2 à 3 ans.
- Pour ces terres légères, la dose d’entretien se situe autour de 350 à 500 unités maximum de valeur neutralisante.
Cas particulier des prairies permanentes
Stratégie d’apport : source groupe chaulage du COMIFER
- Si pH < 5.5, il est nécessaire de lever les risques importants de toxicité aluminique.
L’apport de redressement se justifie pour amener le pH au delà de 5.5 et par rapport à la composition de la flore à moyen terme.
- Si pH compris entre 5.5 et 6.3, l’entretien du pH sera justifié pour le maintien de la composition floristique, la pérennité de la prairie, la productivité en lien avec l’augmentation de l’azote absorbé, l’effet sur les légumineuses.
- Au delà de 6.3, la surveillance du pH reste d’actualité en particulier en cas de forte fertilisation azotée.
Remarque : les valeurs indiquées ci-dessus se réfèrent à un pHeau moyen sur l’horizon 0/10 cm.
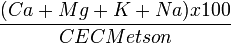 (2)
(2)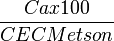 (2)
(2)